研究背景:
开角型青光眼(OAG)是全球范围内不可逆性失明的主要病因,其特征为视网膜神经节细胞(RGCs)进行性变性,并由此导致视野缺损。在 OAG 的遗传致病因素中,MYOC 基因突变约占成年发病型原发性开角型青光眼的 2%~4%,以及青少年型开角型青光眼的 10%。MYOC 相关青光眼通常表现为眼压(IOP)显著升高。此类突变会导致肌纤蛋白错误折叠并在小梁网(TM)内蓄积,诱发内质网应激(ER stress),损害小梁网功能,最终引起眼压升高—— 而眼压升高是青光眼进展的核心驱动因素。传统青光眼治疗手段包括药物、激光及手术,主要目的为降低眼压,但均无法直接纠正其根本的分子缺陷。基因治疗是一种极具前景的策略,可靶向针对 MYOC 相关开角型青光眼的病因进行干预。
本研究旨在评估腺相关病毒 DJ 型(AAV‑DJ)载体介导的靶向 MYOC 短发夹 RNA(shMYOC),在 MYOC P370L 转基因青光眼小鼠模型(Tg‑MYOC P370L)中,治疗由MYOC 突变相关开角型青光眼(OAG)的疗效。
方法:
携带人MYOC 基因 Pro370Leu 突变的转基因小鼠,采用CRISPR/Cas9 系统构建。
简要流程:将 Cas9 信使 RNA(mRNA)、单导向 RNA(sgRNA)与供体 DNA 共同注射入小鼠受精卵。sgRNA 引导 Cas9 在小鼠H11 基因座处产生双链断裂,从而将CAG-3×Flag-hMYOC-P370L-polyA表达载体插入该位点。H11 基因座位于Eif4enif1与Drg1基因之间,是外源启动子驱动基因高效表达的安全位点。采用 PCR 对首建鼠进行基因分型,并通过 DNA 测序验证基因型。
术后评估指标包括:肌纤蛋白(myocilin)聚集、内质网应激标志物表达、眼压(IOP)、房水流畅度、视网膜神经节细胞(RGC)存活及视觉功能。小鼠先用3% 异氟烷诱导麻醉,随后以2.5% 异氟烷维持麻醉。参照既往 established 实验方案,在麻醉诱导后 4~6 分钟,使用Tonolab 大小鼠回弹式眼压计(Icare Finland Oy,赫尔辛基)测量眼压(IOP)。
所有纵向眼压检测均在同一昼夜时间段内完成。测量时眼压计与地面垂直,探针垂直对准角膜中心。每只眼连续测量 6 次,由眼压计自动计算平均值,作为该眼的眼压值。每只眼重复测量 3 轮,记录全部数据。
所有动物实验均遵循ARVO 眼科与视觉研究动物使用声明,并经首都医科大学实验动物福利与伦理委员会批准(批准号:AEEI-2017-11、AEEI-2023-037)。本实验室动物设施通过国际实验动物评估和认可委员会(AAALAC)认证。
结果:
本研究中,我们采用经瞳孔玻璃体腔入路向前房注射 AAV-DJ–shMYOC(1×10¹⁰ vg / 眼),特异性靶向人源MYOC 转基因。与 CRISPR 等基因编辑工具不同,shRNA 在mRNA 水平发挥作用,不会影响不表达靶蛋白细胞的整体基因表达谱,因此具有更优的安全性。
鉴于多数 MYOC 突变集中于C 端区域,我们将 shRNA 设计为靶向编码序列的上游区域,从而可实现对多种 MYOC 突变体的广谱敲低。我们首先在体外验证了候选 shMYOC 的敲低效率,并筛选出效果最佳的载体用于后续体内实验。
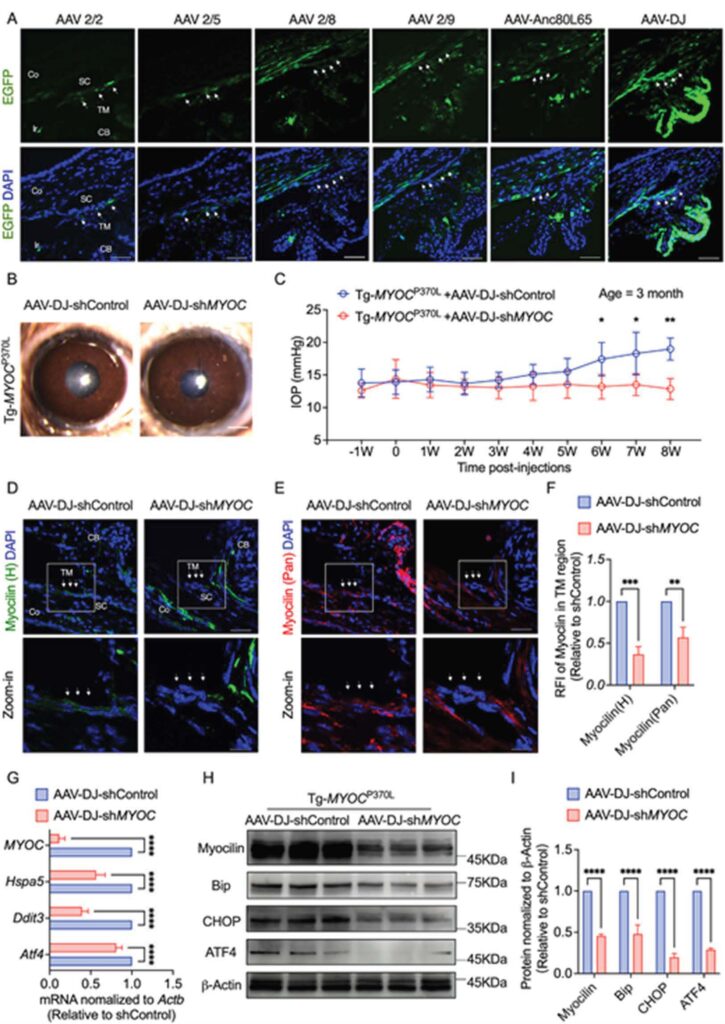
AAV-DJ–shMYOC 注射未在前房引发明显炎症反应。对 3 月龄小鼠给予 AAV-DJ–shMYOC 干预后,可有效阻止对照组(AAV-DJ–shControl)出现的随年龄增长的眼压升高。
注射 2 个月后,与 shControl 对照组相比,shMYOC 干预眼的小梁网(TM)组织中人肌纤蛋白(myocilin)表达显著降低。
此外,对包含虹膜根部、角膜及邻近巩膜组织的 “TM 环” 样本提取 RNA 与蛋白后检测发现:与 AAV-DJ–shControl 相比,AAV-DJ–shMYOC 转染可在mRNA 和蛋白水平显著降低肌纤蛋白(MYOC)及内质网应激标志物的表达,包括BiP(Hspa5)、CHOP(Ddit3)和 ATF4(Atf4)。
以上结果证实:在成年 Tg-MYOCP370L 小鼠体内,AAV-DJ–shMYOC 可高效降低小梁网中肌纤蛋白表达,并缓解内质网应激。
结论:
本研究为AAV-DJ 介导的 MYOC 基因沉默提供了有力证据,表明该策略可作为肌纤蛋白相关性青光眼极具前景的基因治疗方法。通过直接靶向疾病的遗传病因,该疗法有望实现长期稳定的眼压控制与视神经保护。后续研究应着力解决临床转化中的关键问题,为最终应用于临床治疗奠定基础。
致谢
本研究受北京市自然科学基金(7254321)、国家自然科学基金(82130029)及国家自然科学基金(82201170)资助。